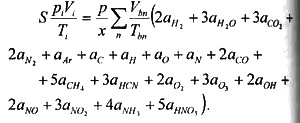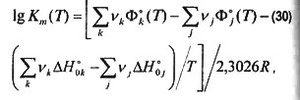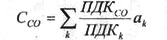МОДЕЛИРОВАНИЕ ГОРЕНИЯ СМЕСИ В ДВС С ИСКРОВЫМ ЗАЖИГАНИЕМ С ОБРАЗОВАНИЕМ ТОКСИЧНЫХ ВЕЩЕСТВ В РАМКАХ МНОГОЗОННОЙ МОДЕЛИ
В.И. Жгутова, М.Ю. Свердлов, Д.Д. Матиевский, П.К. Сеначин
ВВЕДЕНИЕ
Выбросы вредных веществ в атмосферу двигателями внутреннего сгорания (ДВС) различных типов вносят заметный вклад в создание напряженной экологической обстановки в России, которая имеет тенденцию к ухудшению [1-5]. Поэтому перед двигателестроителями и эксплутационниками стоит задача резкого уменьшения влияния техногенного воздействия на природу, обусловленного выделяемыми в атмосферу с продуктами сгорания ДВС вредными веществами. При этом важным является такая организация рабочего процесса ДВС, при которой будут гарантированы минимальные вредные выбросы.
В этой связи особое значение имеют исследования, анализирующие основы физических процессов в ДВС, определяющие полноту и состав продуктов сгорания, так как технически неэффективно и экономически нецелесообразно переделывать уже готовые двигатели под ужесточающиеся нормы на токсичность отработавших газов. В этом плане системы нейтрализации отработавших газов также используются для борьбы со следствием, а не с причиной возникновения токсичных компонентов.
Целями настоящей работы являются: разработка надежных методов расчета состава продуктов, образующихся в процессе сгорания различных топлив в ДВС с искровым зажиганием; оценка экологических свойств продуктов сгорания; расчет процесса сгорания для различных режимов работы двигателя и поиск оптимальных путей снижения вредных выбросов отработавших газов ДВС. Расчет рабочего процесса, необходимым этапом которого является расчет равновесного состава, позволяет: во-первых, проследить динамику образования веществ в процессе сгорания; во-вторых, определить влияние различных факторов на образование вредных веществ еще на стадии проектирования двигателя.
Специфической особенностью процесса горения в ДВС является возникновение температурного градиента в продуктах горения, который может достигать нескольких сотен градусов. Поэтому химические процессы не ограничиваются фронтом пламени и продолжаются в продуктах горения. Прежде всего, к ним относятся процессы диссоциации продуктов фронтального горения и составляющих окислителя (или атмосферного воздуха). В результате количество выбросов вредных веществ в атмосферу определяется не только процессом фронтального горения, но и дальнейшей эволюцией продуктов горения, вплоть до момента их выброса в атмосферу.
Поскольку основным недостатком существующих подходов является то, что в них рассматривается однозонная, в лучшем случае двухзонная модель (зона свежей смеси и зона продуктов сгорания), нами предпринята попытка моделирования процесса сгорания в ДВС с искровым зажиганием в рамках многозонной модели, то есть с учетом Махе-эффекта. Используемый в работе термодинамический метод позволяет определить равновесный состав продуктов сгорания для любых заданных начальных условий (состава смеси, температуры, давления) с учетом диссоциации. Разработан универсальный алгоритм, который позволяет проводить расчеты для любых углеводородных топлив, в состав которых может входить также азот и кислород, и их смесей.
МАТЕМАТИЧЕСКАЯ МОДЕЛЬ
Основные положения математической модели и результаты расчетов изложены в работе [б], где рассмотрены проблемы взрыва газа в бомбе постоянного объема в рамках многозонного приближения. В настоящей работе эта модель предлагается для описания процессов горения в ДВС с искровым зажиганием. Новая математическая модель включает более строгие уравнения энергии для продуктов горения в зонах и балансное уравнение динамики давления в системе, учитывающие индивидуальные зависимости теплоемкостей компонентов смеси в зонах от температуры. Исходные данные для разработки математической модели и расчета равновесного состава продуктов горения можно найти в работах и монографиях [7-16].
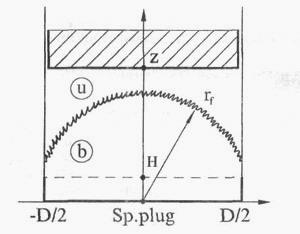
Рис. 1. Фронтальное распространение турбулизированного пламени в симметричной камере сгорания:
Sp. Plug- точка поджигания смеси
Пусть в момент закрытия впускного клапана (j
a
заданы параметры состояния смеси ра, Та, Va, коэффициент избытка воздуха a
и составляющие атмосферного воздуха a
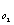 =0.20642, a
=0.20642, a
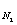 =0.76952,
=0.76952, 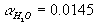 ,
, 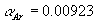 ,
, 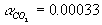 [17]. Концентрация (мольная доля) топлива af при этом определяется заданным коэффициентом избытка воздуха af = l/[l +
[17]. Концентрация (мольная доля) топлива af при этом определяется заданным коэффициентом избытка воздуха af = l/[l + 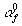 -l)]. Параметры концентрации в свежей смеси остаются неизменными. В продуктах горения учитывается 19 компонентов: О2, N2, Н2О, Аr, СО2, СН4 ,Н2, С, O3, О, N, Н, ОН, СО, NO, NO2, HCN, NH3, HNO3 ,концентрации которых изменяются по ходу процесса. Рассматриваемый рабочий объем системы состоит из одной зоны перед фронтом пламени (свежей смеси) и N зон в продуктах горения (рис. 1).
За начальные параметры приняты параметры системы в момент зажигания j
i. Переход системы в состояние j
i из состояния j
а осуществляется по политропе, близкой к закону Пуассона:
-l)]. Параметры концентрации в свежей смеси остаются неизменными. В продуктах горения учитывается 19 компонентов: О2, N2, Н2О, Аr, СО2, СН4 ,Н2, С, O3, О, N, Н, ОН, СО, NO, NO2, HCN, NH3, HNO3 ,концентрации которых изменяются по ходу процесса. Рассматриваемый рабочий объем системы состоит из одной зоны перед фронтом пламени (свежей смеси) и N зон в продуктах горения (рис. 1).
За начальные параметры приняты параметры системы в момент зажигания j
i. Переход системы в состояние j
i из состояния j
а осуществляется по политропе, близкой к закону Пуассона:
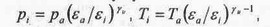
где e
а
= Va/Vc, e
i, = Vi/Vc - степени сжатия (действительная и после зажигания),
Vc = (П/2)rD2/(e
-1)- объем камеры сгорания. Объемы в моменты закрытия впускного клапана и зажигания определяются
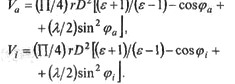
Математическая модель процесса сгорания смеси в ДВС с искровым зажиганием с учетом равновесного состава продуктов горения включает уравнения:
- объема системы и его динамики (для аксиального механизма):
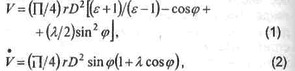
сохранения массы и баланса объема системы:
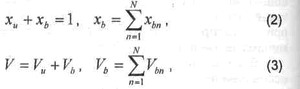
состояния свежей смеси и продуктов горения в зонах:
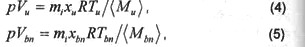
энергии свежей смеси и продуктов горения в зонах
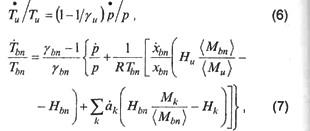
динамики давления:
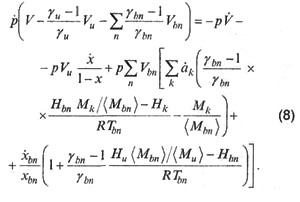
массовой скорости горения на фронте пламени:
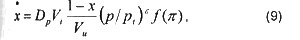
функции площади поверхности пламени
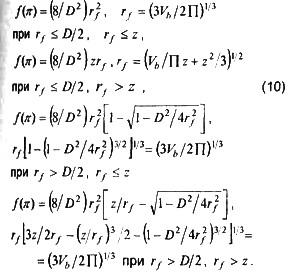
В этих уравнениях обозначено: p -давление; V- объем; Т- температура; mi = piVi(Mu)/RTi –масса смеси; М- молекулярная масса, средняя молекулярная масса рассчитывается с учетом всех j-x компонентов в свежей смеси и к-х компонентов в продуктах горения 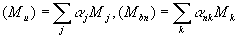 - средние молекулярные массы свежей смеси и продуктов горения в зонах; х=m/mi,-массовая доля; g
- коэффициент Пуассона, для свежей смеси и продуктов сгорания определяется с использованием уравнения Майера g
=ср(Т)/[ср (T)-R], теплоемкость смеси идеальных газов вычисляется по формуле
- средние молекулярные массы свежей смеси и продуктов горения в зонах; х=m/mi,-массовая доля; g
- коэффициент Пуассона, для свежей смеси и продуктов сгорания определяется с использованием уравнения Майера g
=ср(Т)/[ср (T)-R], теплоемкость смеси идеальных газов вычисляется по формуле 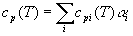 , для индивидуальных веществ (компонентов свежей смеси и продуктов сгорания) значения cpi заданы таблицей с шагом 100 К, для текущей температуры cpi(T) рассчитываются методом интерполяции (с использованием кубического сплайна); R- универсальная газовая постоянная;
, для индивидуальных веществ (компонентов свежей смеси и продуктов сгорания) значения cpi заданы таблицей с шагом 100 К, для текущей температуры cpi(T) рассчитываются методом интерполяции (с использованием кубического сплайна); R- универсальная газовая постоянная; 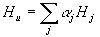 ,
, 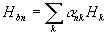 мольная энтальпия свежего газа и продуктов горения в зонах;
мольная энтальпия свежего газа и продуктов горения в зонах;

мольная энтальпия
j-ой компоненты свежей смеси и k-ой компоненты в продуктах горения; 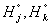 , - мольная энтальпия при стандартной температуре T°
;
, - мольная энтальпия при стандартной температуре T°
;  - нормальная скорость пламени для смеси стехиометрического состава;
- нормальная скорость пламени для смеси стехиометрического состава; 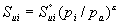 - нормальная скорость пламени в момент зажигания;
- нормальная скорость пламени в момент зажигания; 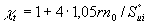 - фактор турбулизации пламени; r - радиус кривошипа;
- фактор турбулизации пламени; r - радиус кривошипа; 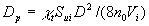 - динамический параметр; D - диаметр поршня;
- динамический параметр; D - диаметр поршня; 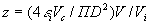 - текущее значение координаты поршня. Индексы i, и, b, п, j, к относятся к начальному состоянию, свежей смеси, продуктам горения, номеру зоны в продуктах, соответствующих компонентам в свежей смеси и продуктах горения соответственно. Точки над переменными обозначают производную по углу поворота коленчатого вала, например, ρ = dp/dj
.
В приведенной системе уравнений для мольных долей компонентов смеси в каждой из зон и их производных справедливо:
- текущее значение координаты поршня. Индексы i, и, b, п, j, к относятся к начальному состоянию, свежей смеси, продуктам горения, номеру зоны в продуктах, соответствующих компонентам в свежей смеси и продуктах горения соответственно. Точки над переменными обозначают производную по углу поворота коленчатого вала, например, ρ = dp/dj
.
В приведенной системе уравнений для мольных долей компонентов смеси в каждой из зон и их производных справедливо:
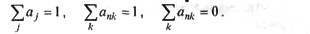
Продукты горения разбиваются на зоны, внутри которых температура усредняется по объемам. Для каждой из зон в процессе фронтального горения и вплоть до момента окончания горения (выброса) рассчитывается равновесное состояние продуктов.
Математическая модель процесса представляет собой систему дифференциальных уравнений, для решения которой используется метод Рунге-Кутта четвертого порядка. При этом на каждом шаге счета рассчитывается равновесный состав продуктов горения в каждой зоне. После окончания горения до момента открытия выпускного клапана расчет ведется аналогично, за исключением уравнения (11),•которое принимает вид: х = 0.
В системе уравнений для расчета равновесного состава продуктов горения константами являются: суммарное число атомов в одном моле свежей смеси и число атомов кислорода в начале процесса в единицах числа Авогадро NA:
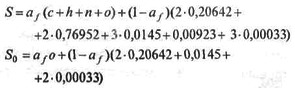
и отношение числа атомов соответственно С, Η, Ν, Аr к числу атомов кислорода
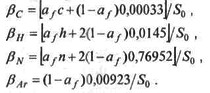
Система уравнений для расчета равновесного состава включает уравнения:
- материального баланса (через мольные доли)
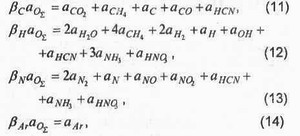
где число атомов кислорода в одном моле продуктов горения
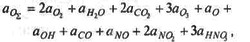
- суммы мольных долей компонентов смеси
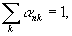
- химического равновесия
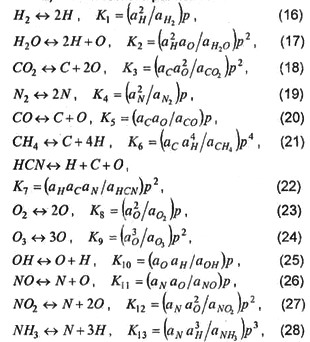
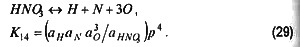
В данной системе уравнений справедливо сохранение числа атомов в продуктах горения
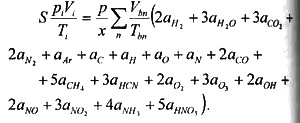
Константы химического равновесия К1- К14 - являются функциями текущей температуры продуктов сгорания и рассчитываются на основе термодинамического уравнения для каждой m-й реакции (уравнения изобары реакции):
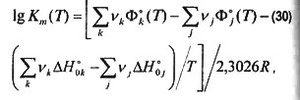
где vj, vk- стехиометрические коэффициенты m-й реакции; 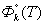 и
и 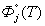 - приведенные энергии Гиббса соответствующих реагентов, рассчитываются для текущей температуры на основе аппроксимирующих уравнений;
- приведенные энергии Гиббса соответствующих реагентов, рассчитываются для текущей температуры на основе аппроксимирующих уравнений; 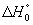 - тепловой эффект m-й реакции при абсолютном нуле температуры.
Система уравнений для расчета равновесного состава продуктов является нелинейной, для ее решения используется метод Ньютона.
Продукты горения разбиваются на 10 зон. В расчетах варьируется: коэффициент избытка воздуха а, угол опережения зажигания j
i , степень сжатия ε, частота вращения коленчатого вала п0. В качестве модельных топлив приняты: водород Н2, метан СН4, пропан С3Н8, бутан С4Н10, гептан С7Н16, изооктан C8H18, бензин ( смесь изооктана и гептана).
В результате расчета процесса получаем: 1) температуру в каждой зоне и соответственно градиент температур в продуктах; 2) полный состав продуктов горения в каждой зоне; 3) суммарный выход продуктов, позволяющий оценить количество выбросов вредных веществ (СО, NO, ΝΟ2, HCN , NH3, HNO3), образующихся в процессе сгорания.
Результаты расчетов показывают (все данные приводятся на момент окончания горения), что основными токсичными составляющими продуктов горения из рассматриваемых являются оксид углерода СО и окислы азота NOX, доля остальных компонентов незначительна. Из окислов азота образуется практически только N0, доля NO2 незначительна и составляет меньше 1% от общего количества всех окислов азота.
- тепловой эффект m-й реакции при абсолютном нуле температуры.
Система уравнений для расчета равновесного состава продуктов является нелинейной, для ее решения используется метод Ньютона.
Продукты горения разбиваются на 10 зон. В расчетах варьируется: коэффициент избытка воздуха а, угол опережения зажигания j
i , степень сжатия ε, частота вращения коленчатого вала п0. В качестве модельных топлив приняты: водород Н2, метан СН4, пропан С3Н8, бутан С4Н10, гептан С7Н16, изооктан C8H18, бензин ( смесь изооктана и гептана).
В результате расчета процесса получаем: 1) температуру в каждой зоне и соответственно градиент температур в продуктах; 2) полный состав продуктов горения в каждой зоне; 3) суммарный выход продуктов, позволяющий оценить количество выбросов вредных веществ (СО, NO, ΝΟ2, HCN , NH3, HNO3), образующихся в процессе сгорания.
Результаты расчетов показывают (все данные приводятся на момент окончания горения), что основными токсичными составляющими продуктов горения из рассматриваемых являются оксид углерода СО и окислы азота NOX, доля остальных компонентов незначительна. Из окислов азота образуется практически только N0, доля NO2 незначительна и составляет меньше 1% от общего количества всех окислов азота.
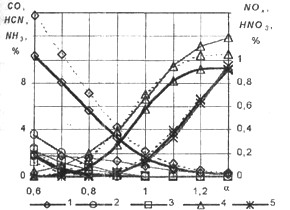
Рис. 2. Зависимость концентрации токсичных веществ от а: 1 - СО (для водорода СО
*102), 2 - HCN* 104 (для водорода HCN* 107), 3 – NH3* 103, 4 - NOX, 5 - ΗΝΟ3* 107
Зависимость концентрации токсичных веществ от коэффициента избытка воздуха а приведена на рис. 2 для метана (сплошная линия), бензина-92 (пунктир) и водорода (сплошная тонкая линия), j
i =-20 град, п.к.в., ε=7, n0=2000 об/мин, Tа=298 К, ра=1 атм; для остальных рассматриваемых топлив имеет тот же характер. При обогащении смеси увеличивается выход СО, HCN и ΝΗ3, причем достаточно резко при уменьшении коэффициента избытка воздуха до a
= 0,6-0,8; доля NOх и HNO3 здесь минимальна. При обеднении смеси (a
>0,8) возрастает выход NOx и ΗΝΟ3 и при а>1 их концентрации достигают максимального значения. Оценка токсичности смеси с помощью комплексного показателя, учитывающего не только долю каждого токсичного составляющего в отработавших газах, но и их вредность, приведенную к одному веществу, позволяет сделать вывод о составе смеси значение коэффициента избытка воздуха a
), обеспечивающем минимальную токсичность на данном режиме работы двигателя.
Оценка суммарной токсичности метана, отнесенная к оксиду углерода и определяемая по формуле
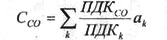
приведена на рис. 3 для смесей различного состава, на котором показана доля, вносимая оксидом углерода СО в суммарную токсичность и поскольку доля
HCN , ΝΗ3, HNO3 в продуктах очень незначительна, оставшаяся доля в суммарной токсичности принадлежит окислам азота NOx.
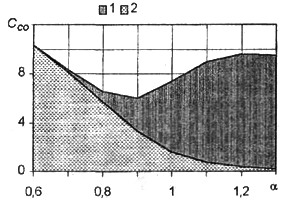
Рис. 3. Суммарная токсичность метана (1) и доля, вносимая СО
(2)
Влияние вида топлива на концентрацию токсичных составляющих приведено на рис. 4-8, горение смеси стехиометрического состава, j
i=-20 град. п.к.в., e
=7, nо=2000 об/мин, Tа=298 К, ра=1 атм.
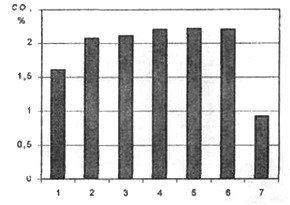
Рис. 4. Зависимость концентрации СО от вида топлива: 1 - метан, 2 - пропан, 3 -бутан, 4 - гептан, 5 - изооктан, 6 - бензин-92, 7 - водород (*10
2)
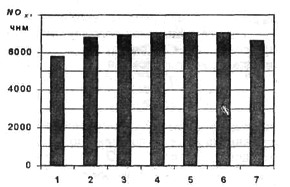
Рис. 5. Зависимость концентрации
NOX от вида топлива: 1 - метан, 2 - пропан, 3 -бутан, 4 - гептан, 5 - изооктан, 6 - бензин-92,7 - водород
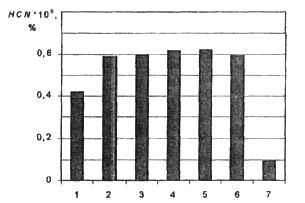
Рис. 6. Зависимость концентрации
HCN от вида топлива: 1 - метан, 2 - пропан, 3 -бутан, 4 - гептан, 5 - изооктан, 6 - бензин-92, 7-водород (*Ί07)
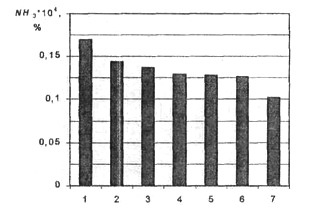
Рис. 7. Зависимость концентрации
NH3 от вида топлива: 1 - метан, 2 - пропан, 3 -бутан, 4 - гептан, 5 - изооктан, 6 - бензин-92, 7 - водород (*103)
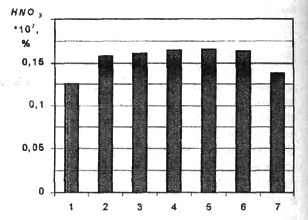
Рис. 8. Зависимость концентрации
HNO3 от вида топлива: 1 - метан, 2 - пропан, 3 -бутан, 4 - гептан, 5 - изооктан, 6 - бензин-92,7 – водород
Оценка суммарной токсичности рассматриваемых топлив, отнесенная к оксиду углерода, приведена на рис. 9, из которого можно сделать вывод, что из рассматриваемых топлив метан и водород являются наиболее перспективными в экологическом смысле.
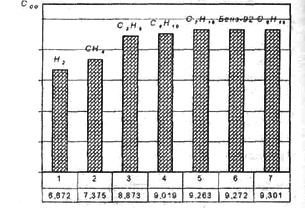
Рис. 9. Суммарная токсичность топлив для ос=1
Зависимость концентраций веществ от угла опережения зажигания при горении метана приведена на рис. 10-14 для различных показателей коэффициента избытка воздуха и разной частоты вращения, ε=7, n0=2000 об/мин (сплошная линия) и n0=6000 об/мин (пунктир), Tа=298 К, ра=1 атм. Влияние частоты вращения коленчатого вала на выброс токсичных веществ незначительно, можно отметить тенденцию к увеличению выброса всех токсичных составляющих при малой частоте вращения и рост влияния частоты вращения по мере уменьшения угла опережения зажигания.Уменьшение опережения зажигания приводит к сокращению концентраций рассматриваемых вредных веществ. Изменение угла опережения зажигания практически не влияет на концентрацию CO.
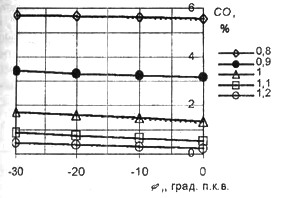
Рис. 10. Зависимость концентрации СО от угла опережения зажигания
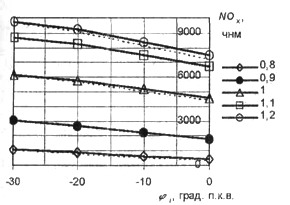
Рис. 11. Зависимость концентрации
NOx от угла опережения зажигания
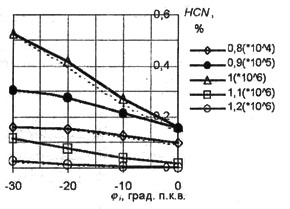
Рис. 12. Зависимость концентрации
HCN от угла опережения зажигания
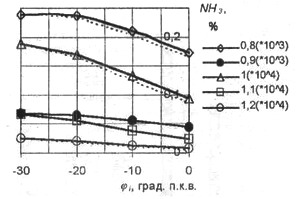
Рис. 13. Зависимость концентрации
NH3 от угла опережения зажигания
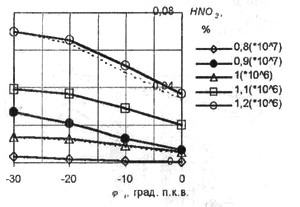
Рис. 14. Зависимость концентрации
HNO3 от угла опережения зажигания
Концентрация NOx значительно снижается с уменьшением угла опережения зажигания j
i при работе двигателя на обедненных и стехиометрических смесях (a
³
1), на обогащенных смесях изменение j
i практически не влияет на концентрацию NOх. С уменьшением опережения зажигания можно отметить некоторое уменьшение HNO3 при работе на обедненных смесях и HCN и ΝΗ3 при сгорании обогащенных смесей.
Влияние степени сжатия на концентрацию веществ приведено на рис. 15-17 для смесей разного состава; горение метана, j
i =-20 град, п.к.в., nо=2000 об/мин, Tа=298 К, pa=1 атм. Независимо от состава смеси, изменение степени сжатия практически не влияет на выход СО. С повышением степени сжатия токсичность отработавших газов несколько возрастает из-за повышения концентраций NOx, HCN, NH3 и HNO3.
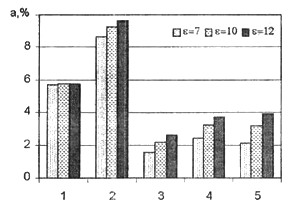
Рис. 15. Влияние степени сжатия на концентрацию веществ, a
=0,8: 1 - СО, 2 –
NOx* 102, 3 - HCN*105, 4 – NH3*104, 5 -HNO3* 1010
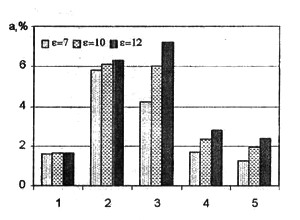
Рис. 16. Влияние степени сжатия на концентрацию веществ, a
=1: 1-СО, 2 -ΝΟχ*10, 3 - HCN*107, 4 – NH3*105, 5 -HNO3*108
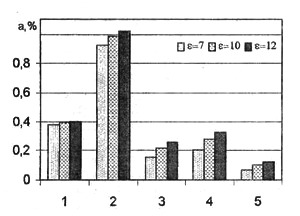
Рис. 17. Влияние степени сжатия на
концентрацию веществ, a
=1,2: 1-CO, 2-NOx, 3 - HCN*107, 4 -NH3*105, 5 - HNO3*106
На рис. 18-22 приведена зависимость концентраций веществ от температуры Ta и давления ра (ра=1 атм - сплошная линия, ра=2 атм - пунктир) в момент закрытия впускного клапана для случая сгорания метана при j
i=-20 град. п.к.в., nо=2000 об/мин.
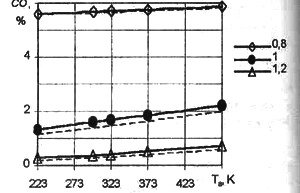
Рис. 18. Зависимость концентрации СО от температуры
Ta
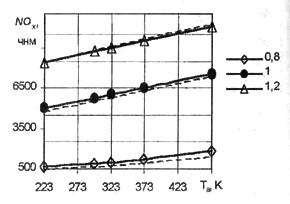
Рис. 19. Зависимость концентрации
NOx от температуры Ta
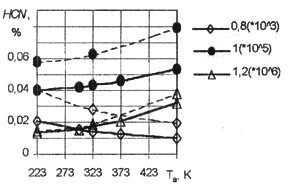
Рис. 20. Зависимость концентрации
HCN от температуры Тa
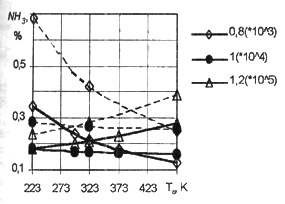
Рис. 21. Зависимость концентрации
NH3 от температуры Тa
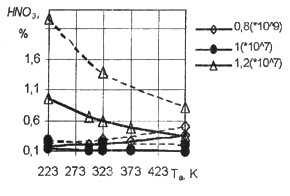
Рис. 22. Зависимость концентрации
HNO3 от температуры Тa
Видно, что при горении стехиометрических и обедненных смесей незначительно возрастает концентрация СО с увеличением Та, и при увеличении ра наблюдается тенденция к некоторому снижению концентраций, на обогащенных смесях влияние Тa и ра отсутствует. Концентрация NOX в продуктах сгорания увеличивается досточно резко с увеличением Тa на стехиометрических и обедненных смесях, на обогащенных смесях влияние Тa уменьшается. С увеличением ра наблюдается снижение концентраций NOX при горении обогащенных и стехиометрических смесей, на обедненных смесях влияние ра практически отсутствует. Поскольку основными токсичными составляющими являются СО и NOX можно сделать вывод об увеличении токсичности отработавших газов с возрастанием температуры Та.
Изменением параметра, входящего в фактор турбулизации, можно варьировать продолжительность сгорания, влияние которой на образование токсичных составляющих приведено на рис. 23, где по оси абсцисс отложена продолжительность сгорания в градусах угла п.к.в., горение метена, a
=1, j
i =-20 град. п.к.в., ε=7, nο=2000 об/мин, Tа=298 К, ра=1 атм. Увеличение продолжительности сгорания приводит к уменьшению концентраций всех рассматриваемых токсичных составляющих продуктов сгорания. Это можно объяснить тем, что после прохождения в.м.т. в конце процесса сгорания температура продуктов снижается. Соответственно снижается и количество вредных веществ, выбрасываемых в атмосферу, среди которых важнейшими являются оксид углерода и оксиды азота.
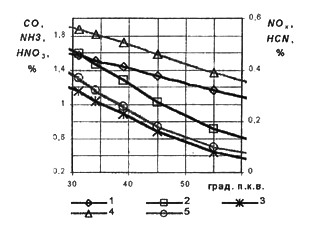
Рис. 23. Влияние продолжительности сгорания на образование вредных веществ: 1- СО,
2- NH3*105, 3- HNО3*108, 4 - NOx, 5 - НСN*106
ВЫВОДЫ
- На основе уточненных уравнений энергии построена новая многозонная математическая модель фронтального горения топливно-воздушных смесей различного состава в ДВС с искровым зажиганием с учетом процессов химического равновесия в произвольном числе зон продуктов горения (то есть с учетом Махе-эффекта).
- Проведены численные исследования образования вредных веществ, включающих оксид углерода, оксиды азота, аммиак, азотную и синильную кислоту, при сгорании различных видов топлив, в том числе метана (или природного газа), пропана, бутана, гептана, изооктана, бензина-92 и водорода, при различных начальных давлениях и температурах и варьирование коэффициента избытка воздуха, угла опережения зажигания, частоты вращения коленчатого вала и степени сжатия.
ЛИТЕРАТУРА
- Звонов В.А. Токсичность двигателей внутреннего сгорания. 2-е изд. М.: Машиностроение, 1981. 160 с.
- Сигал И.Я. Защита воздушного бассейна при сжигании топлива. 2-е изд. Л.: Недра, 1988. 312 с.
- Кривоногов Б.М. Повышение эффективности сжигания газа и охрана окружающей среды. Л.: Недра, 1986, 280 с.
- Горбунов В.В., Патрахальцев Н.Н. Токсичность двигателей внутреннего сгорания / Учеб. пособие. М.: Изд-во РУДН, 1998.214 с.
- Жегалин О.И., Лупачев П.Д. Снижение токсичности автомобильных двигателей. М.: Транспорт, 1985. 120 с.
- Моделирование взрыва газа в бомбе постоянного объема с учетом равновесного состава продуктов горения / В.И. Жгутова, М.Ю. Свердлов, П.К. Сеначин, Д.Д. Матиевский // Вестник АлтГТУ им. И.И. Ползунова. 1999. № 2. С. 127-136.
- Гурвич A.M., Шаулов Ю.Х. Термодинамические исследования методом взрыва и расчеты процессов горения. М.: МГУ, 1995. 167 с.
- Стюард Р. Бринкли мл. Методы вычисления термодинамических параметров продуктов сгорания. // Процессы горения / Под ред. Б. Льюиса, Р.Н. Пиза, Х.С. Тейлора. М.: Гос. изд-во физ.-мат. лит-ры, 1961, с. 67-94.
- Математическая теория горения и взрыва / Я.Б. Зельдович, Г.И. Баренблатт, В.Б. Либрович, Г.М. Махвиладзе. М.: Наука, 1980.478 с.
- Щетинков Е.С. Физика горения газов. М.: Наука, 1965.740 с.
- Kovasznay L.S.G. A Comment on Turbulent Combustion // Jet Propulsion, 1956. Vol. 26, No. 6, p. 485.
- Кора R.D., Hollander F.H., Hollander B.R., Kimura H. Combustion Temperature, Pressure and Products at Chemical Equilibrium // S.A.E. Progress in Technology (Digital Calculation of Engine Cycles), 1964, Vol. 7, p. 10-37.
- Agrawal D.D., Gupta C.P. Computer Program for Constant Pressure or Constant Volume Combustion Calculations in Hydrocarbon-Air Systems // Trans. ASME, 1977, Ser. A 99-2, p. 246-254.
- Сталл Д., Вестрам Э., Зинке Г. Химическая термодинамика органических соединений. М.: Мир, 1971. 807 с.
- Термодинамические свойства индивидуальных веществ: Спр. изд. в 4-х томах / Под ред. В. П. Глушко. М.: Наука, 1978.
- Рябин В.А., Остроумов М.А., Свит Т.Ф. Термодинамические свойства веществ: Справочник. Л.: Химия, 1977. 392 с.
- Миртов Б.А. Газовый состав атмосферы Земли и методы его анализа. М.: АН СССР, 1961.262 с.
- Льюис Б., Эльбе Г. Горение, пламя и взрывы в газах. М.: Изд-во иностр. лит., 1948. 447 с; 2-е изд. М.: Мир, 1968. 592 с.


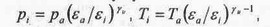
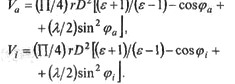
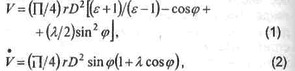
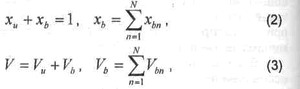
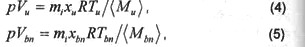
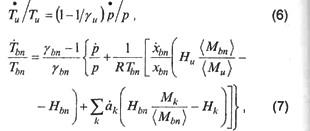
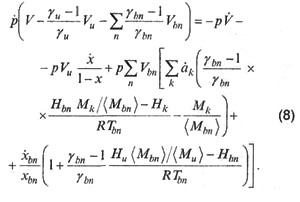
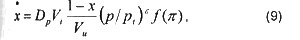
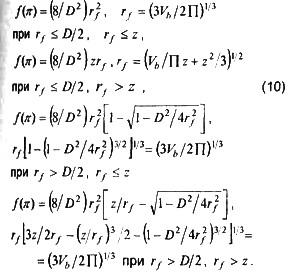

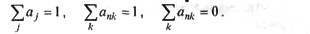
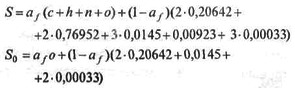
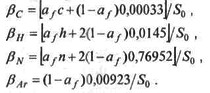
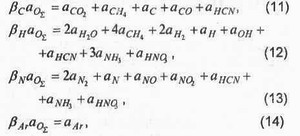
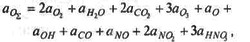
![]()
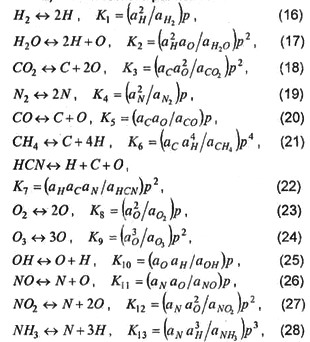
![]()